Dra. Carla Sofía González Arocha
Introducción
El glaucoma neovascular (GNV) es una complicación asociada a patologías isquémicas que representa un reto clínico para todo oftalmólogo [1-3]. A pesar del avance en las terapias con medicamento anti-factor de crecimiento endotelial vascular (anti-VEGF), la pérdida visual continúa siendo frecuente debido a una obstrucción del ángulo por rubeosis y proliferación fibrovascular, lo que bloquea la salida del humor acuoso [2,3].
El tratamiento médico, el uso de anti-VEGF y la terapia láser, constituyen la primera línea para reducir la presión intraocular (PIO); sin embargo, en casos avanzados, la intervención quirúrgica es necesaria [1,4]. En este contexto, la implantación de dispositivos de drenaje para glaucoma (DDG) se ha consolidado como la opción preferida gracias a sus resultados favorables en el manejo del GNV [5-7]. El implante de glaucoma PAUL® (PGI) es uno de los dispositivos no valvulados más recientes, con mercado CE desde el 2018, y en México a partir del 2025.
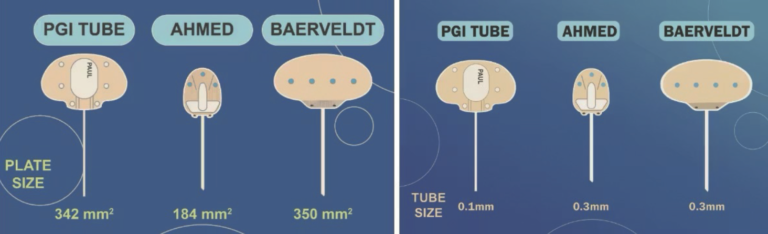
A diferencia de los implantes de Baerveldt (BGI) y Ahmed (AGI), el PGI presenta un tubo de menor calibre (diámetro interno: 0.127 mm; diámetro externo: 0.467 mm), sin comprometer el tamaño del cuerpo valvular (342 mm2); esto permite ofrecer un control más refinado de la PIO con menor riesgo de complicaciones [8].
Diversos estudios han demostrado que los dispositivos de drenaje para glaucoma no valvulados constituyen una intervención segura y eficaz en distintas formas de glaucoma; sin embargo, en el GNV se ha sugerido que los implantes valvulados ofrecen ventajas en el periodo posoperatorio temprano, debido a un menor riesgo de hipotonía inicial, un control más rápido de la presión intraocular (PIO) y una menor complejidad quirúrgica [9–11]. No obstante, el Ahmed versus Baerveldt Study (ABC), al comparar ambos tipos de dispositivos, demostró una superioridad de los implantes no valvulados en términos de control de la PIO a largo plazo.
Objetivo
Actualizar a los oftalmólogos sobre los implantes no valvulados de nueva generación, en particular el implante de glaucoma PAUL®, mediante el análisis de la literatura científica reciente, con el fin de optimizar la toma de decisiones clínicas y el manejo quirúrgico del GNV.
Metodología
Se realizó una revisión narrativa y descriptiva de la literatura científica actual relacionada con el implante de glaucoma PAUL®, y se analizaron estudios clínicos, series de casos y reportes recientes, con el objetivo de integrar una visión crítica y actualizada de su uso en escenarios clínicos complejos.
Resultados
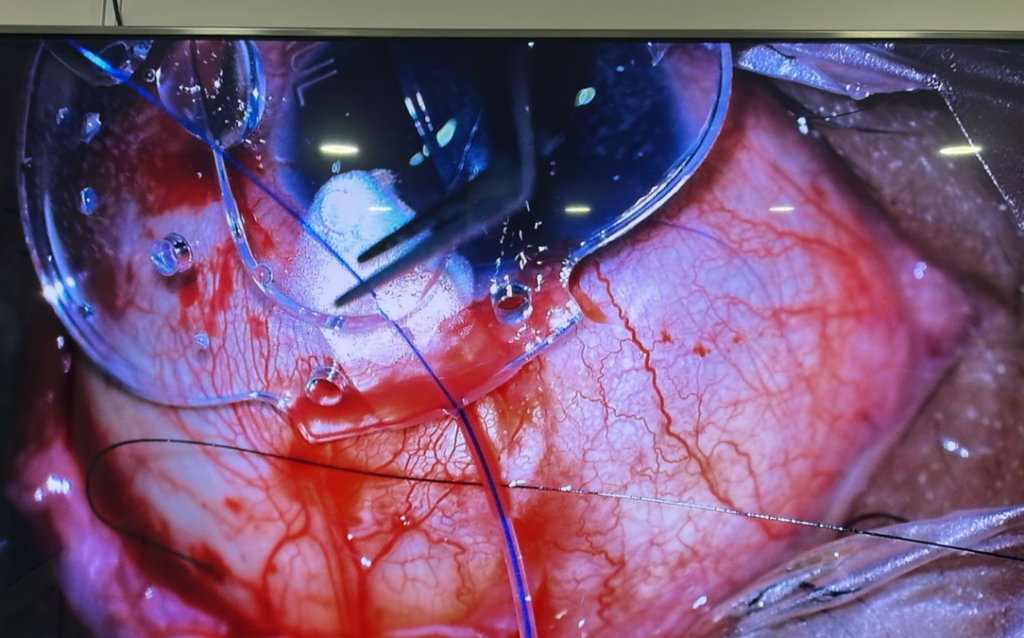
1. Técnica quirurgica: en la mayoría de los casos, el PGI se coloca en el cuadrante superotemporal, aunque puede colocarse en cuadrantes alternativos. Se coloca una sutura de tracción con Vycril 7.0; la exposición quirúrgica se realiza mediante una peritomía conjuntival y de tenon en el cuadrante seleccionado; se aplica mitomicina C a una concentración de 0.5 mg/mL durante dos a cinco minutos en el área destinada a la colocación de la placa del implante; se lava con 20-30cc de solución salina; se comprueba flujo del tubo con solucion salina y se introduce una sutura de prolene 6-0 dentro del tubo con el objetvio de restringir el flujo; la placa del PGI se introduce por debajo de los músculos rectos y se fija a la esclera mediante suturas de nylon 9–0, seda 7-0 o prolene 9-0 aproximadamente a 10 mm por detrás del limbo corneal; se utiliza una cánula calibre 25 para crear un túnel hacia la cámara anterior 4-5 milimetros del limbo quirúrgico; tras recortar el tubo a la longitud requerida, este se introduce a través del túnel hacia la cámara anterior y se fija mediante una sutura de nylon 9–0 o 10-0 en configuración tipo “caja”; si es posible, el tubo se protege con un injerto de esclera o fascia lata de doble capa, fijado con la ayuda de adhesivo de fibrina o sutura Nylon 10-0; la sutura de Prolene se aloja, habitualmente, en un bolsillo subconjuntival en el cuadrante inferior, o se fija a la cornea; si se observa una mayor salida de flujo o hay riesgo alto de hipotonia, se coloca una sutura de vycril 7-0 o de nylon 9-0 alrededor del tubo para restringir el flujo. El procedimiento concluye con el cierre conjuntival, a partir de dos suturas de nylon 10–0 con nudo corredizo en los extremos, y dos suturas adicionales tipo colchonero con nylon 10–0.
2. Control de la presión intraocular: el PGI logró una reducción significativa de la PIO en GNV, alcanzando una disminución del 53.1 % a los 12 meses (de 27.22 mm Hg en el preoperatorio a 12.95 mmHg) [12].
El análisis de Kaplan–Meier mostró tasas de éxito del 60-80 % para PIO ≤ 21 mmHg, mientras que solo del 10 % para PIO ≤ 12 mmHg [12].
3. Complicaciones: el 39.1 % de los pacientes presentó alguna complicación, siendo las relacionadas con hipotonía las más frecuentes (17 %) [12]. La tasa de hifema se observa en el 8.7 % de los pacientes, presentando dicha complicación durante la primera semana posterior a la cirugía [12]. Un 8.6 % requiere revisión de tubo por dehiscencia conjuntival [12], además, otras complicaciones que se pueden observar son atalamia, uveítis postquirúrgica, infección, erosión conjuntival, obstrucción del tubo, migración o malposición del tubo, diplopia/alteraciones de la motilidad o descompensación corneal.
El 21.7 % de los pacientes continuó recibiendo inyecciones intravítreas (el 8.6 % con fotocoagulación panretiniana) [12]. Es importante mencionar que la sutura de Prolene se sugiere retirar después de las 4 semanas (idealmente alrededor de los 3 meses).
Conclusiones
El implante de glaucoma PAUL® combina un tubo de menor calibre con una placa de gran superficie, comparable a la de otros DDG tradicionales, lo que permite un control eficaz de la PIO sin incrementar riesgo de complicaciones. Gracias a estas diferencias estructurales, los resultados con el PGI son similares o superiores a los reportados en la literatura de otros DDG, con el mismo riesgo de complicaciones [12].
El implante de glaucoma PAUL® se ha consolidado como el implante de elección para el GNV en ojos con potencial visual, gracias a su balance favorable entre eficacia y seguridad.
-
-
-
- Malgi VS, Gawas L, Iyer AS, Rao A. Clinical profile and outcomes of neovascular glaucoma in the era of anti-vascular endothelial growth factor. Indian J Ophthalmol. 2021;69(10):2728–2733. doi:10.4103/ijo.IJO_528_21
- Urbonavičiūtė D, Buteikienė D, Janulevičienė I. A review of neovascular glaucoma: etiology, pathogenesis, diagnosis, and treatment. Medicina (Kaunas). 2022;58(12):1870. doi:10.3390/medicina58121870
- Senthil S, Dada T, Das T, Kaushik S, Puthuran GV, Philip R, et al. Neovascular glaucoma: a review. Indian J Ophthalmol. 2021;69(3):525–534. doi:10.4103/ijo.IJO_1591_20
- Hayreh SS. Neovascular glaucoma. Prog Retin Eye Res. 2007;26(5):470–485. doi:10.1016/j.preteyeres.2007.06.001
- Subasi S, Yuksel N, Karabas VL, Yilmaz Tugan B, Basaran E. Ahmed glaucoma valve implantation for secondary glaucoma post-vitrectomy. Int Ophthalmol. 2022;42(3):847–854. doi:10.1007/s10792-021-02050-2
- Weber C, Hundertmark S, Brinken R, Holz FG, Mercieca K. Erste klinische Ergebnisse mit dem PAUL®-Glaukom-Implantat an der Universitäts-Augenklinik Bonn. Ophthalmologie. 2022;119(12):1267–1274. doi:10.1007/s00347-022-01669-5
- José P, Barão RC, Teixeira FJ, Marques RE, Peschiera R, Barata A, Abegão PL. One-year efficacy and safety of the PAUL glaucoma implant using a standardized surgical protocol. J Glaucoma. 2022;31(3):201–205. doi:10.1097/IJG.0000000000001969
- Weber C, Weinhold L, Walz W, Petrak M, Holz FG, Liegl R, Mercieca K. Sonographic bleb visualisation after PAUL glaucoma implant surgery. Br J Ophthalmol. 2024;108:3168–3174. doi:10.1136/bjo-2024-326168
- Richardson J, Tacea F, Yu J, Yau K, Fenerty C, Au L. The PAUL glaucoma implant in the management of uveitic glaucoma: 3-year follow-up. Eye (Lond). 2024. doi:10.1038/s41433-024-03527-x
- Weber C, Hundertmark S, Stasik I, Holz FG, Mercieca K. Two-year clinical outcomes of the PAUL glaucoma implant in white patients with refractory glaucoma. J Glaucoma. 2024;33(10):808–814. doi:10.1097/IJG.0000000000002457
- Weber C, Schipper P, Walz W, Raming K, Künzel S, Holz FG, Liegl R, Mercieca K. Clinical outcomes of the PAUL® glaucoma implant for secondary glaucoma after vitreoretinal surgery. Ophthalmologica. 2025;243:1–23. doi:10.1159/000543748
- Deubel C, Walz W, Petrak M, Holz FG, Liegl R, Mercieca K, Liegl Née Weber C. Clinical outcomes of the PAUL glaucoma implant for neovascular glaucoma. Graefes Arch Clin Exp Ophthalmol. 2025;263(11):3199–3209. doi:10.1007/s00417-025-06933-3
-
-