Dra. Ayumi Kawakami Campos, Dr. José Antonio Remolina Villarejo
Introducción
Tal vez no nos habíamos dado cuenta, pero como oftalmólogos, ya utilizamos inteligencia artificial todos los días. Cada que un estudio nos ofrece una paleta de colores con aquello que se sale del rango normal, eso fue generado por inteligencia artificial. No hay un señor escondido dentro del equipo que colorea cada espacio del círculo y compara los datos que tiene apuntados en una libreta. Todo esto, desde que una máquina identifique dónde está la fóvea, que mida específicamente el grosor de las células ganglionares, que estime el flujo de sangre dentro de los vasos a partir de imágenes en 2D, entre otras cosas, ¡es inteligencia artificial! Y como se habrán dado cuenta, no se sustituyó a nadie ni nos volvimos obsoletos; nos hicimos más eficientes, objetivos y precisos.
Antecedentes
Actualmente existen alternativas que permiten generar modelos de predicción para saber qué paciente requiere vigilancia estrecha o quién va a tener una evolución favorable. Muchas de estas herramientas que están en desarrollo cuentan con patentes exclusivas o son específicas para ciertas marcas de equipos; sin embargo, algunas ya son gratuitas y podemos acceder a ellas libremente.
Aplicaciones
La literatura referente a inteligencia artificial en oftalmología ha crecido a una velocidad tan rápida que incluso revistas de renombre como Ophthalmology o New England Journal of Medicine tienen ahora suplementos trimestrales o sub-revistas dedicadas exclusivamente a este campo. Al leer estos artículos, es importante tener en mente algunas cosas que nos permiten ser objetivos y juiciosos: los datos con los que se alimentan los algoritmos son imágenes de tomografía de coherencia óptica (OCT), fondo de ojo y biopsias; deben estar perfectamente detallados e incluir la población de donde proceden; es menester saber con qué equipo se tomaron, si fueron calificadas por expertos como normales o anormales, cuántas se utilizaron para entrenar el algoritmo y probar su efectividad.
Después, necesitamos leer a detalle qué modelo de inteligencia artificial usaron: si está validado por un tercero independiente, si los resultados son lógicos o explicables, si hubo efecto de caja negra (cuando no es posible determinar en qué basa su decisión el algoritmo), qué tan aplicable es el algoritmo, y si esto se interpreta en el contexto de un ensayo clínico o en la práctica diaria. (Imagen 1)
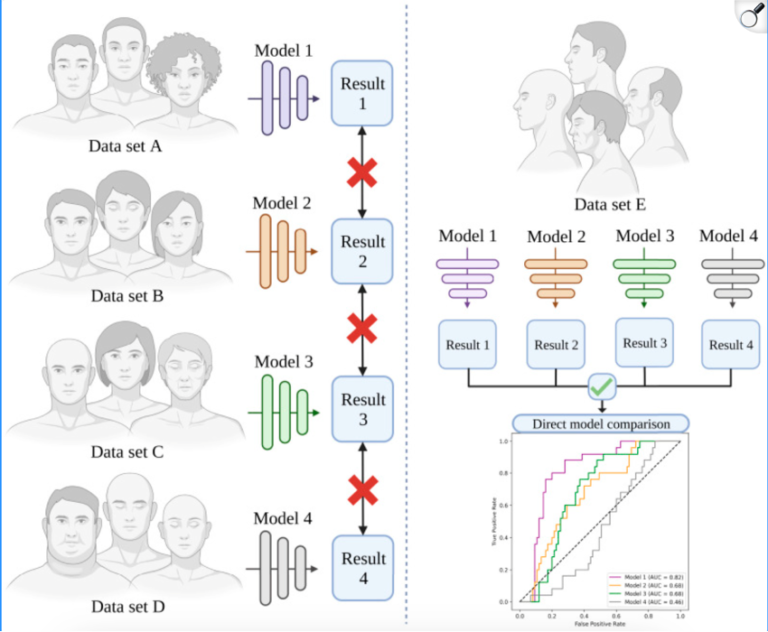
Si tenemos diferentes grupos de pacientes, por ejemplo, de diversos países, edades y antecedentes médicos, en cada país se hace un modelo diferente. Para compararlos, tendríamos que utilizar estos modelos en la misma población y obtener un área bajo la curva en la que cada algoritmo tenga una sensibilidad y especificidad cuantificable.
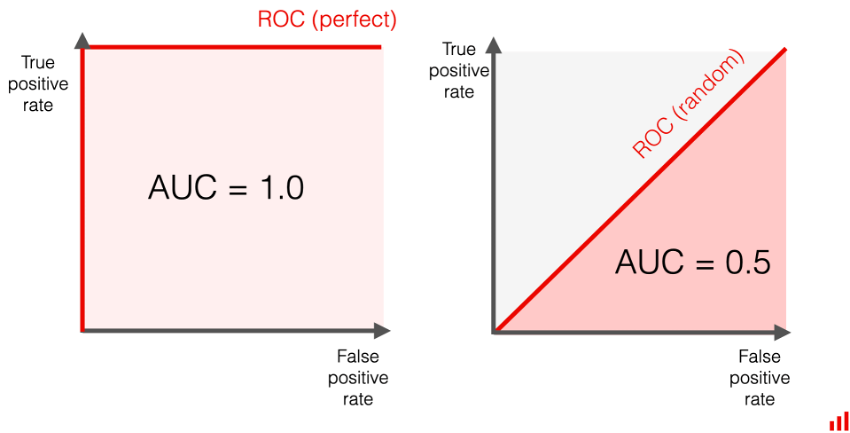
Otro punto que debemos recordar al leer bibliografía de inteligencia artificial es el ROC AUC o área bajo la curva (Receiver Operating Characteristic Area Under the Curve). Este número es un indicador de la relación que hay entre la detección de los verdaderos positivos y los verdaderos negativos. Un modelo bien hecho debe aproximarse al 1; una prueba que tiene un AUC de 0.5 es igual de preciso que aventar una moneda al aire. Algo específico de la IA, es que si el algoritmo arroja un AUC de 1, es porque está mal hecho: ese algoritmo está “sobreentrenado” y no va a ser posible aplicarlo a ninguna imagen que no provenga de los datos con los que se entrenó.
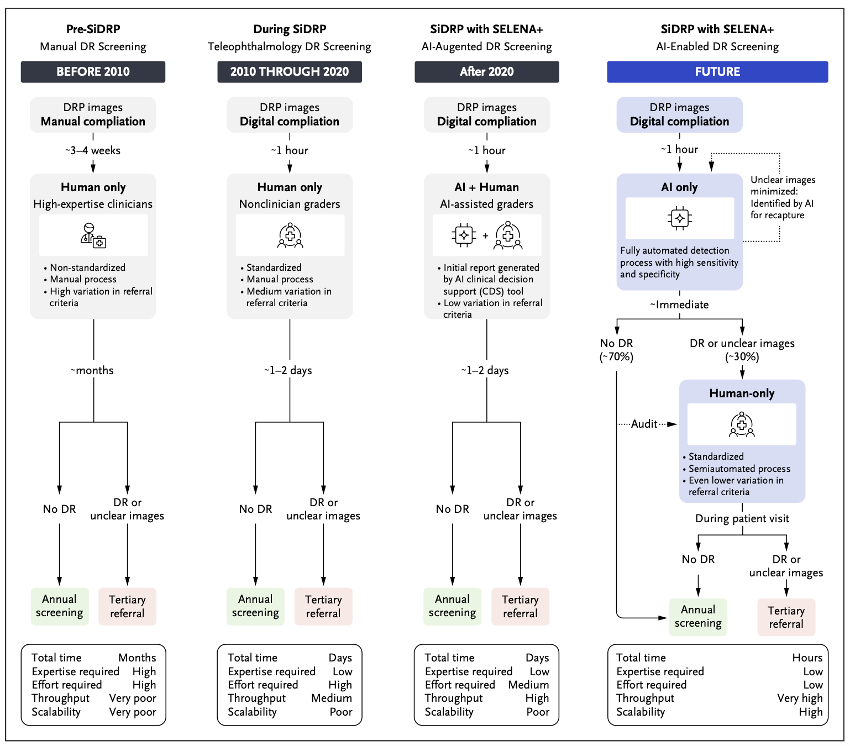
En retina, el diagnóstico asistido por inteligencia artificial ha permitido establecer sistemas de tamizaje autónomo: fuimos el primer rubro en medicina en tener equipos aprobados por la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) para diagnósticos autónomos de retinopatía diabética. A partir del 2023, la Asociación Americana de la Diabetes incluyó en sus guías un suplemento sobre IA en el tamizaje, y tiene excelentes imágenes que nos ayudan a entender cómo funcionan las redes convolucionales neuronales, cómo se lleva a cabo el tamizaje fuera de la clínica y cómo esto podría evitar casos de ceguera.
La agencia europea ha sido más rigurosa para aprobar estos algoritmos; sin embargo, la FDA cuenta con 3 softwares aprobados que pueden incorporarse al flujo de cualquier sistema de salud. Estos son: AEYE-DS (AEYE Health), EyeArt AI screening system (Eyenuk) y LumineticsCore. Algunos requieren cámaras no midriáticas y ofrecen resultados en menos de 1 minuto; no obstante, otros pueden utilizarse en línea, y brindar un resultado positivo o negativo para patología asociada a diabetes mellitus en segundos.
En países como Singapur, se han generado algoritmos con datos de pacientes de todas sus regiones, que permiten detectar retinopatía diabética, degeneración macular y glaucoma. A partir de la IA, cuantificaron en retrospectiva cuánto le tomaba a cada paciente ser atendido y diagnosticado, y lograron una reducción del tiempo (desde el diagnóstico hasta la evaluación por el especialista) de meses a horas.
En la reciente reunión anual de la Association for Research in Vision and Ophthalmology (ARVO), se presentaron más de 58 abstracts relacionadas a inteligencia artificial, estos incluyen: proyectos de automatización en el diagnóstico, optimización de tratamientos, asociación de hallazgos oculares con
enfermedades en otros órganos, predicción de pronóstico,modelos de lenguaje para interacción con pacientes y expediente electrónico, entre otros.
Desafíos
Parte importante de la discusión actual, es su aplicabilidad en países en vías de desarrollo (ya que los algoritmos están generados con datos de pacientes de otras razas y características), el costo operacional de implementar esta tecnología, los sesgos implícitos dentro de la generación de los agentes, la propiedad intelectual de los datos obtenidos y la necesidad de optimizar los resultados acordes a la población en la que se utilicen.
En países en vías de desarrollo como el nuestro, los programas para la formación de especialistas no suelen incluir este tipo de temas. No existe financiamiento público para su generación ni implementación y no tenemos legislación vigente que abarque su aplicabilidad; sin embargo, la inteligencia artificial ha llegado para ser permanente. Adaptarnos a su empleo y ser críticos respecto a su calidad y limitaciones, nos permitirá hacer mejor uso de ella y conservar nuestra máxima de “Primum non nocere”.
Conclusiones
La inteligencia artificial está revolucionando cada aspecto de nuestras vidas. Es un área que será igual o más trascendental que la invención del internet. Particularmente, las ciencias de la salud se beneficiarán de su incorporación en el desarrollo de fármacos, tamizajes, individualización de tratamiento, predicción de evolución, reducción de errores, identificación de patrones y un largo etcétera. Debido a que la oftalmología es un área donde prácticamente todo se puede visualizar, fotografiar o medir, es lógico que sea una de las especialidades pioneras en el rubro. La responsabilidad de conocer a detalle los pormenores de su uso, sus limitaciones y sus beneficios, recae en cada uno de los usuarios e interlocutores.
- Rajesh AE, Davidson OQ, Lee CS, Lee AY. Artificial Intelligence and Diabetic Retinopathy: AI Framework, Prospective Studies, Head-to-head Validation, and Cost- effectiveness. Diabetes Care [Internet]. 2023 Sep 20;46(10):1728–39. Available from: https://diabetesjournals.org/care/article/46/10/1728/153626/Artificial-Intelligence-and-Diabetic-Retinopathy
- Evidently AI Team. How to explain the ROC AUC score and ROC curve? [Internet]. www.evidentlyai.com. 2024. Available from: https://www.evidentlyai.com/classification- metrics/explain-roc-curve
- Gunasekeran DV, Miller S, Hsu W, Lee ML, Wong HT, Lee MT, et al. National Use of Artificial Intelligence for Eye Screening in Singapore. NEJM AI. 2024 Nov 27;1(12).
- Yang Q, Bee YM, Lim CC, Charumathi Sabanayagam, Cheung CYL, Wong TY, et al. Use of artificial intelligence with retinal imaging in screening for diabetes-associated complications: systematic review. EClinicalMedicine [Internet]. 2025 Feb 18 [cited 2025 Mar 22];81:103089–9. Available from: https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(25)00021-5/fulltext
- De Fauw J, Ledsam JR, Romera-Paredes B, Nikolov S, Tomasev N, Blackwell S, et al. Clinically Applicable Deep Learning for Diagnosis and Referral in Retinal Disease. Nature Medicine. 2018 Aug 13;24(9):1342–50.