Área Médica Laboratorios Sophia
Introducción
Controlar y prevenir la inflamación es fundamental para alcanzar resultados óptimos después de una cirugía. La manipulación quirúrgica de las estructuras del segmento anterior propicia la liberación de ácido araquidónico de las membranas celulares, lo que desencadena la síntesis de prostaglandinas y leucotrienos. Estos mediadores inflamatorios hacen que exista una reacción celular y se liberen proteínas. Aunque usualmente hay una autolimitación, la inflamación no tratada puede producir complicaciones como dolor, incomodidad, fotofobia, edema corneal, sinequias, glaucoma y edema macular quístico [1,2].
Inflamación asociada a cirugía ocular
Las cirugías prolongadas o aquellas que implican manipulaciones extensas pueden dar lugar a una inflamación postoperatoria pronunciada. La inflamación posterior a la cirugía se manifiesta mediante la presencia de células en el humor acuoso, flare, fibrina y, ocasionalmente, vasos de los iris ingurgitados. Esta inflamación, aunque generalmente transitoria, puede exacerbarse por material lenticular retenido o por daño a las estructuras intraoculares causado por un lente intraocular implantado [3].
La mayoría de los médicos emplea un régimen de medicamentos antiinflamatorios en el período perioperatorio y, por su amplia actividad antiinflamatoria, los corticoesteroides son típicamente la piedra angular [1].
Uveítis anterior endógena
La uveítis y las enfermedades inflamatorias intraoculares son trastornos potencialmente amenazantes para la visión, que afectan a personas de todas las edades. Anatómicamente, la uveítis puede clasificarse en uveítis anterior, intermedia, posterior y panuveítis. Además, puede categorizarse según factores etiológicos como infecciosa, no infecciosa, neoplásica y postoperatoria. Dicha enfermedad puede presentarse de forma aislada o como parte de un síndrome ocular o sistémico. Su patogenia exacta sigue sin ser clara; sin embargo, la evidencia ha demostrado que está mediada por el sistema inmunológico y es influida por factores endógenos. Puede manifestarse en individuos con predisposición genética en combinación con un desencadenante ambiental [4].
La práctica clínica actual enfatiza el tratamiento de la inflamación con corticosteroides tópicos, y la velocidad de resolución se asocia con una menor probabilidad de secuelas. En casos de uveítis anterior muy severa pueden administrarse con una frecuencia de hasta 30 minutos [5].
Desde el reconocimiento de la actividad antiinflamatoria de los extractos adrenocorticales a principios de la década de 1940, la hidrocortisona (cortisol), el principal glucocorticoide secretado por la corteza suprarrenal humana, y varios derivados sintéticos, han demostrado ser útiles en estados de enfermedades autoinmunes e inflamatorias oculares [6].
Difluprednato
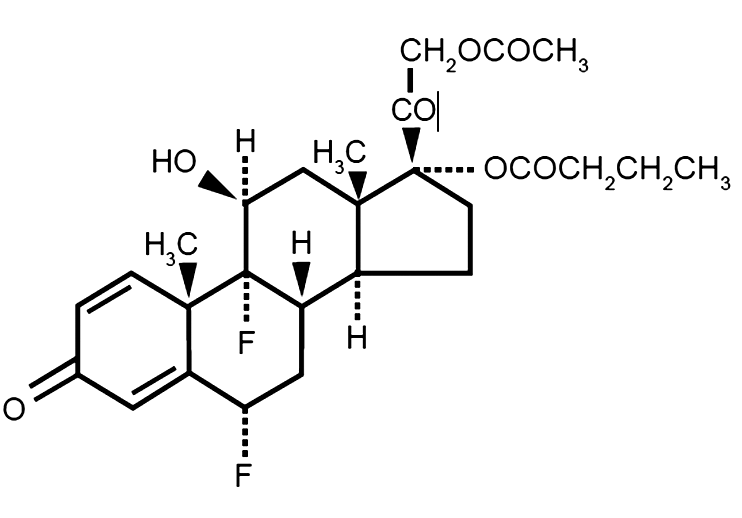
El difluprednato es un medicamento sintético difluorinado derivado de la prednisolona. Originalmente fue desarrollado para aplicaciones dermatológicas por Mitsubishi Pharma; no obstante, con base en sus resultados clínicos, el producto fue catalogado como un corticosteroide “muy potente”. En su formulación dermatológica, el difluprednato 0.05 % fue 4 veces más potente que el acetato valerato de prednisolona 0.4 %, y 3,200 veces más fuerte que la prednisolona 0.5 %, usando la vasoconstricción periférica. En esta presentación, su potencia fue aproximadamente la misma que la betametasona [1,7]. La molécula obtiene su potencia mediante la fluoración en las posiciones C6 y C9. Su actividad antiinflamatoria se ve adicionalmente aumentada por la sustitución del grupo hidroxilo en la posición 17 por un butirato, mientras que su lipofilicidad y, por ende, su penetración corneal, se incrementa mediante la sustitución del grupo hidroxilo en la posición 21 por un acetato [8].
Como todos los corticosteroides, el difluprednato inhibe la respuesta inflamatoria frente a diversos agentes desencadenantes y puede retrasar el proceso de cicatrización. Inhibe el edema, la deposición de fibrina, la dilatación capilar, la migración de leucocitos, la proliferación capilar, la proliferación de fibroblastos, la deposición de colágeno y la formación de cicatriz asociada a la inflamación [9].
No existe una explicación universalmente aceptada sobre el mecanismo de acción de los corticosteroides oculares; sin embargo, se considera que actúan mediante la inducción de proteínas inhibidoras de la fosfolipasa A2, conocidas en conjunto como lipocortinas. Estas regulan la biosíntesis de mediadores inflamatorios potentes como las prostaglandinas y los leucotrienos, al inhibir la liberación de su precursor común: el ácido araquidónico, el cual se libera de los fosfolípidos de membrana a través de la acción de la fosfolipasa A2 [9].
Dado el número limitado de esteroides oftálmicos potentes disponibles, el difluprednato fue formulado como una preparación tópica. En junio de 2008, la emulsión de difluprednato al 0.05 % fue aprobada por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para el tratamiento de la inflamación y el dolor asociados con cirugía ocular [8], mas fue hasta 2018 que se aprobó la primera emulsión de difluprednato al 0.05 % en México por la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) bajo la indicación de “Tratamiento de la inflamación y dolor asociado a cirugía ocular y en el tratamiento de uveítis anterior endógena”.
Método
Inflamación postquirúrgica
Se llevaron a cabo dos estudios pivote idénticos, aleatorizados, enmascarados doblemente y controlados con placebo, para evaluar la emulsión oftálmica de difluprednato al 0.05 % y su vehículo en 219 pacientes con inflamación ocular posterior a cirugía de catarata (conteo de células en cámara anterior ≥1+). Los pacientes no tenían antecedentes de glaucoma, hipertensión ocular, aumento de la PIO relacionado con esteroides, abrasión o úlcera corneal, y presentaban una PIO <24 mmHg el día después de la cirugía [9].
Los pacientes recibieron una gota de la emulsión oftálmica de difluprednato al 0.05 % (BID, QID o del placebo), a partir del día siguiente a la cirugía y durante 14 días, seguido por un periodo de disminución progresiva de hasta 14 días adicionales. El principal criterio de eficacia fue la proporción de pacientes con conteo de células en cámara anterior (CA) igual a 0. El criterio secundario fue la proporción de pacientes sin dolor o molestia [9]. Difluprednato administrado QID fue superior al placebo en la resolución de células en CA y en la reducción del dolor o molestia a partir del día 8 [9].
Uveítis anterior endógena
Se realizaron 2 estudios fase 3, aleatorizados, controlados, enmascarados doblemente y con control activo, diseñados para demostrar no inferioridad. En total, se aleatorizaron 200 sujetos con uveítis anterior endógena, de los cuales 106 recibieron emulsión oftálmica de difluprednato al 0.05 % cuatro veces al día. La población consistió en 180 sujetos (94 con emulsión oftálmica de difluprednato y 86 con acetato de prednisolona) [9].
Los pacientes con uveítis anterior endógena leve a moderada recibieron emulsión oftálmica de difluprednato al 0.05 % cuatro veces al día, o suspensión oftálmica de acetato de prednisolona al 1 % ocho veces al día durante 14 días. A partir del día 14 y durante las siguientes dos semanas, los participantes comenzaron una reducción gradual de la dosis, disminuyendo progresivamente a la mitad el número de aplicaciones diarias en cada etapa. Desde el día 28 en adelante, el tratamiento adicional quedó a discreción del investigador [9].
El criterio de valoración principal de eficacia fue el cambio desde el valor inicial en la calificación de células en la cámara anterior al día 14 entre el grupo de difluprednato y el grupo de prednisolona. La calificación de células en la cámara anterior se determinó utilizando una escala de 5 puntos, que va de 0 (≤1 célula) a 4 (>50 células). El margen de no inferioridad utilizado fue de 0.5 unidades, lo que significa que el límite superior del intervalo de confianza bilateral del 95 % debía ser menor a 0.5 para establecer la no inferioridad [9]. La proporción de sujetos con aclaramiento de células en la cámara anterior (recuento celular = 0) al día 14 fue del 52 % en ambos estudios. En el día 42, las tasas de aclaramiento fueron del 62 % y del 70 % [9].
La recaída se definió como un recuento celular en la cámara anterior ≤ 5 en el día 14, que aumentó a un recuento celular > 10 en visitas posteriores. En general, pocos sujetos (7) presentaron recaídas en estos estudios (4 en el grupo de prednisolona y 3 en el grupo tratado con difluprednato). Las recaídas con difluprednato ocurrieron en los días 21 y 42, y en el grupo de prednisolona en los días 35 y 42, alcanzando calificaciones celulares similares a las observadas en los valores iniciales [9].
Resultados
Los corticosteroides tópicos, especialmente los de alta potencia como la dexametasona, pueden provocar un aumento de la presión intraocular (PIO). La hipertensión ocular suele presentarse una semana después de la administración repetida, y puede ser mucho más pronunciada en ojos con glaucoma. La elevación sostenida de la PIO está asociada con daño al nervio óptico, lo que puede conducir a defectos en el campo visual y a una posible disminución de la agudeza visual. Otros efectos incluyen la formación de cataratas subcapsulares posteriores y una mayor predisposición a infecciones oculares secundarias [8].
Las extensas pruebas clínicas han demostrado que la emulsión de difluprednato al 0.05 % provoca una elevación de la PIO en una pequeña minoría de pacientes. Este incremento se resolvió en todos los casos tras la suspensión del medicamento o mediante el uso de soluciones hipotensoras tópicas. Comparado con betametasona administrada con la misma frecuencia, la incidencia de elevación de la PIO fue igual entre ambos grupos, lo que indica un perfil de seguridad aceptable. Los datos de los ensayos fase 1 muestran que los eventos adversos fueron leves y transitorios. Asimismo, los datos de seguridad de otros estudios indican que el difluprednato es bien tolerado tras cirugías oculares y en el tratamiento de la uveítis anterior [8].
Conclusiones
El difluprednato, un corticosteroide sintético de alta potencia con propiedades estructurales que favorecen su penetración corneal, ha demostrado ser eficaz en el control de la inflamación postquirúrgica y en la uveítis anterior, con un perfil de seguridad aceptable frente a esteroides tradicionales como la prednisolona o la dexametasona. Su capacidad para lograr una resolución más rápida de células en cámara anterior y del dolor ocular subraya su relevancia clínica.
La introducción de esta nueva sal en México amplía las alternativas disponibles y ofrece un tratamiento más potente y eficaz para el control de la inflamación ocular. Esta innovación implica mayor accesibilidad local y disponibilidad de un medicamento, lo que representa un avance en términos de equidad en la atención oftalmológica. En perspectiva, el uso de difluprednato puede transformar el manejo clínico, no solo optimizando los resultados visuales postoperatorios, sino también ofreciendo un recurso valioso para el control de enfermedades inflamatorias crónicas. Será necesario impulsar estudios locales que confirmen su efectividad en la población mexicana, fomentar su inclusión en guías clínicas nacionales y evaluar su impacto en la práctica diaria.
- C. Mithal, S. Singh, S. Gupta y S. Mithal, «Difluprednate: an overview,» Delhi Journal of Ophthalmology, vol. 23, nº 3, pp. 165-168, 2012.
- B. Jain y M. Shrivastawa, «To compare the safety and efficacy of difluprednate 0.05% emulsion and prednisolone acetate 1% in the post operative inflammation following cataract extraction with iol implantation,» J of Evoluion of Med and Dent Sci, vol. 3, nº 53, pp. 12341-12343, 2014.
- U. Pleyer, Immune Modulation and Anti-Inflammatory Therapy in ocular Disorders, New York: Springer, 2014.
- Yang, Ming-Ming et al. “The roles of genetic factors in uveitis and their clinical significance.” Retina (Philadelphia, Pa.) vol. 34,1 (2014): 1-11.
- Foster, C Stephen et al. “Durezol (Difluprednate Ophthalmic Emulsion 0.05%) compared with Pred Forte 1% ophthalmic suspension in the treatment of endogenous anterior uveitis.” Journal of ocular pharmacology and therapeutics : the official journal of the Association for Ocular Pharmacology and Therapeutics vol. 26,5 (2010): 475-83. doi:10.1089/jop.2010.0059
- J. D.Bartlett, Clinical Ocular Pharmacology, 5 ed., St. Louis, Missouri: Butterworth-Heinemann, 2008, pp. 221,226-229,235,,236.
- Center for Drug Evaluation and Research, «Application Number: 22-212 Pharmacology Review(s),» 26 Diciembre 2007. [En línea]. Available: https://www.accessdata.fda.gov/drugsatfda_docs/nda/2008/022212s000_PharmR.pdf. [Último acceso: 11 Julio 2022].
- K. N. Jamal, «The role of difluprednate ophthalmic emulsion in clinical practice,» Clinical Ophthalmology, vol. 3, pp. 381-390, 2009.
- Novartis Pharmaceuticals Canada Inc., «Product Monograph Durezol,» Quebec, 2018.