Dr. Irving A. Domínguez Varela, Dr. Oscar F. Miranda Gómez
Introducción
El uso de la luz con fines terapéuticos (fototerapia) se remonta a 1903, cuando el Dr. N. Finsen trató a más de mil pacientes con tuberculosis cutánea. [1] Pasaron aproximadamente 60 años, hasta la década de 1960, para que el Dr. E. Mester acuñara el término de fotobiomodulación moderna, utilizando el concepto de bioestimulación mediante láseres de baja intensidad [2].
Actualmente existen múltiples reportes sobre la aplicación de la bioestimulación en diversas áreas de la medicina. Entre sus usos se incluyen el alivio del dolor y la inflamación en condiciones como fibromialgia, osteoartritis y lesiones deportivas. En odontología, se usa para mejorar la sensibilidad postoperatoria; y, de manera destacada, en dermatología, para el tratamiento de alopecia, acné, herpes y la cicatrización de úlceras cutáneas, entre otros [2].
Las distintas aplicaciones que tiene la luz como tratamiento en la retina se conocen como Terapias Regenerativas Retinianas con Láser y Luz (RELITE, por sus siglas en inglés). Estas se subdividen en cuatro categorías principales relacionadas con los efectos físicos y bioquímicos buscados con el aumento de temperatura: terapia fototérmica, regeneración del EPR (terapia de fotomicrodisrupción), procesos fotoquímicos (terapia fotoquímica) y fotobiomodulación (FBM) [3].
La FBM en la retina se ha utilizado para distintas entidades patológicas como edema macular diabético (EMD), retinopatía del prematuro, coroidopatía central serosa, retinitis pigmentosa, neuropatía óptica hereditaria de Leber, ambliopía y toxicidad retiniana inducida por metanol. De esas condiciones, solo el EMD cuenta con ensayos clínicos controlados fase 2. El resto se ha sostenido con estudios piloto, series de caso o reportes de caso, sin evidencia clínica sólida que respalde un beneficio anatómico o funcional en estas enfermedades hasta la fecha [4,5]. La evidencia clínica más sólida disponible corresponde al uso de la FBM en la degeneración macular asociada a la edad (DMAE). La FBM es una biotecnología establecida, no invasiva y basada en energía de luz, la cual promueve el metabolismo celular y reduce la inflamación del tejido [6].
Metodología
Se realizó una revisión sistemática de la evidencia básica y clínica sobre las aplicaciones de la fotobiomodulación y sus efectos en la retina, así como en la DMAE seca. Para la búsqueda se utilizaron las siguientes palabras clave: laser therapy, light therapy, retinal rejuvenation therapy, thermal stimulation retina, photobiomodulation, subthreshold laser y photodynamic therapy (retina OR mácula). Se descartaron estudios que no fueran sobre DMAE.
Resultados
Para conocimiento de los autores, al día 20 de octubre de 2025, se encontraron un total de 98 artículos, de los cuales cinco eran ensayos clínicos controlados que utilizaban la FBM en la DMAE seca. Se hallaron 30 revisiones y el resto correspondían a cohortes retrospectiva, series de casos y reportes de caso.
1.Mecanismos de acción
Sus efectos son a través de activación de señales en cascadas biológicas, que se han documentado a partir de modelos experimentales y clínicos:
La luz infrarroja cercana (NIR, por sus siglas en inglés) es absorbida por centros redox del CcO (hemea/heme a3 y centros CuA/CuB), lo que facilita la disociación de óxido nítrico (NO) inhibitorio y/o altera el estado redox de dichos centros. Esto restaura/acelera el flujo de electrones, incrementa el bombeo protónico y eleva Δψm (potencial de membrana mitocondrial), aumentando la síntesis de ATP y generando una señalización redox transitoria (ROS, Ca2+, AMPc, NO) que activa rutas de supervivencia, proliferación y anti-inflamación [5].
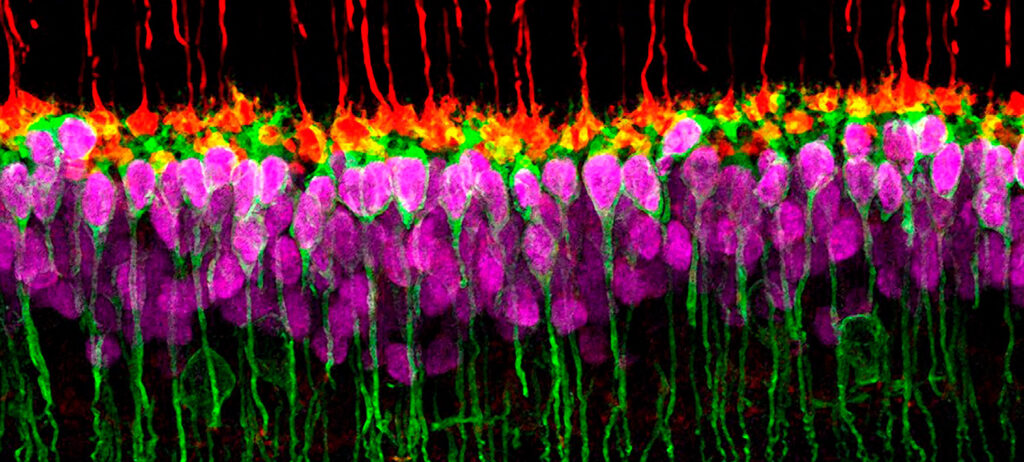
La enzima citocromo C oxidasa (CcO), complejo IV de la cadena respiratoria mitocondrial, es un importante fotoaceptor intracelular y transductor de fotoseñales para longitudes de onda de luz roja (600-750 nm) a infrarroja cercana (750 – 1100 nm) (FR/NIR) y se considera un mecanismo primario subyacente al efecto de la FBM (Figura 1).
El CcO es el aceptor de electrones terminal en la cadena respiratoria: CcO contiene dos centros de cobre (CuA y CuB) y dos centros de hemo (heme-a y heme-a3) que absorben la luz FR/NIR. En las células normóxicas sanas, la actividad primaria de CcO da como resultado un aumento del transporte de electrones y, en consecuencia, un aumento de la producción de ATP y una disminución en el ROS.
En condiciones de estrés hipóxico/inhibición, el NO puede unirse reversiblemente al heme a3 / CuB y bloquear la transferencia de electrones. Fotones de onda roja/NIR pueden liberar NO (fotodisociación), devolviendo la actividad catalítica de CcO y la respiración mitocondrial [7].
1.1.Producción transitoria de ROS como mensajero:
Un ligero aumento pasajero de especies reactivas (ROS) se genera como subproducto del aumento en el flujo electrónico. Esas ROS actúan como segundos mensajeros (no necesariamente tóxicos) activando rutas de señalización redox dependientes (NF-κB, Nrf2, PI3K/Akt, etc.), que promueven supervivencia, proliferación y expresión génica protectora. En células con estrés oxidativo, las ROS totales pueden decrementarse tras tratamientos repetidos (restaurando la homeostasis) [5,7].
1.2. Modulación de Ca²⁺ y canales iónicos (rutas paralelas)
La FBM también puede afectar canales iónicos (p. ej. TRP/TRPV), provocando entrada de Ca²⁺ y activación de cinasas y factores de transcripción. Parte de los efectos terapéuticos se explica por la suma de la mejora bioenergética más las señales iónicas [5].
2. Longitudes de onda
La fotobiomodulación (FBM) emplea diversas longitudes de onda (LO) dentro del espectro de luz visible e infrarroja cercana (550–850 nm). Cada una con mecanismos de acción específicos según su rango de emisión. [6,8]
-
-
-
-
-
-
- LO de 850 nm (NIR): impulsa la transferencia de electrones (CuA), estimula la actividad metabólica (ATP) e inhibe la inflamación y muerte celular.
- LO de 660 nm (roja): promueve la unión de oxígeno (CuB), estimula la actividad metabólica (ATP) e inhibe la inflamación y muerte celular.
- LO de 590 nm (amarilla): inhibe la expresión de VEGF y promueve la generación de óxido nítrico.
-
-
-
-
-
No todos los dispositivos emplean la totalidad de las longitudes de onda disponibles [6,8].
3. Aparatos de FBM disponibles
Al momento existen dos aparatos de FBM disponibles en el mercado, autorizados para tratar a los pacientes con DMAE seca.
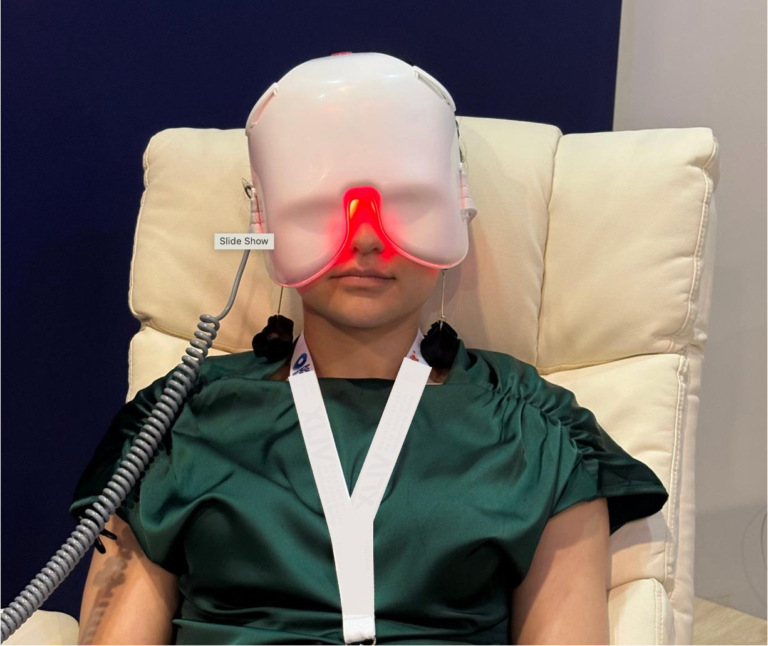
A) Eye-light® (Espansione Group S.p.A., Bologna, Italy): cuenta con certificado de la “Conformité Européenne” (CE). El tratamiento se realiza de forma simultánea en ambos ojos, permitiendo que el paciente permanezca sentado o recostado, gracias al diseño ergonómico del dispositivo, que consiste en una máscara ligera y de fácil colocación. Eye-light® utiliza 2 longitudes de onda (630 y 590 nm) divididos en 2 fases. El protocolo de tratamiento consta de dos fases: en la fase 1, se aplica luz amarilla (590 nm) de forma continua con los ojos cerrados durante 300 segundos, seguido de una emisión pulsada con los ojos abiertos durante 60 segundos. En la fase 2, se repite el mismo procedimiento utilizando luz roja (630 nm). La duración total de la sesión es de aproximadamente 12 minutos, y cada ciclo terapéutico comprende 8 sesiones, distribuidas en 2 sesiones por semana durante 4 semanas. Un segundo ciclo puede realizarse entre 4 y 6 meses después de completar el primero [8].
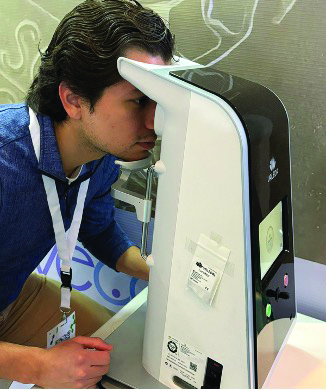
B) Valeda® Light Delivery System (LumiThera, Inc., Poulsbo, WA, USA): autorizado (no aprobado) por la “Food and Drug Administration” (FDA). El tratamiento se realiza de forma unilateral, iniciando con el ojo derecho. El dispositivo Valeda® emplea tres longitudes de onda (590, 660 y 800 nm) que actúan de manera complementaria sobre los tejidos retinianos. El protocolo terapéutico se compone de cuatro fases, con una duración total aproximada de 250 segundos por ojo. En la fase 1, se aplica luz amarilla (590 nm) y luz infrarroja cercana (800 nm) en modo pulsado durante 35 segundos, con los ojos abiertos. La fase 2 consiste en la aplicación de luz roja (660 nm) en modo continuo durante 90 segundos, con los ojos cerrados. La fase 3 repite el esquema de la fase 1, y la fase 4 reproduce las condiciones de la fase 2. Se administran en una serie de 9 sesiones de FBM durante 3 a 5 semanas, y se repiten cada 4 meses [6] (Figura 3).
4. Evidencia básica/preclínica
En un modelo animal de degeneración retiniana, Lu et al. (2017) demostraron que la FBM con luz de 670 nm mejora la función mitocondrial de las células de Müller (aumentando COX5a y ΔΨm) y disminuye la expresión de mediadores inflamatorios como CCL2, IL-1β e IL-6. Esto reduce la activación de microglía y macrófagos inducida por el daño foto-oxidativo. Los hallazgos sugieren que la luz roja puede modular la respuesta glial y atenuar la inflamación retiniana mediante la restauración de la bioenergética celular [9].
En el estudio de Begum et al. (2013), realizado en un modelo murino de degeneración macular relacionada con la edad inducida por luz intensa, el tratamiento con luz de 670 nm incrementó la expresión de citocromo c oxidasa (complejo IV) y disminuyó marcadores inflamatorios como complemento C3, TNF-α e IL-1β en la retina. Estos hallazgos sugieren que la FBM restaura la función mitocondrial y reduce la inflamación asociada al daño foto-oxidativo, apoyando su potencial terapéutico en enfermedades degenerativas oculares [10].
5. Evidencia clínica
5.1 Estudios clínicos
TORPA 1 y 2
Los estudios realizados en Toronto consistieron en dos series de casos intervencionales prospectivas, publicadas en 2012 y 2017, respectivamente. En el ensayo TORPA 1, se evaluó la agudeza visual mejor corregida (AVMC) según ETDRS, la sensibilidad al contraste y la estabilidad de la fijación en 18 ojos con DMAE tras 18 sesiones de FBM, utilizando una longitud de onda de 670 nm. Se incluyeron ojos en estadios 2–4 de AREDS de pacientes de 50 años o más, con AVMC entre 20/200 y 20/20. Se excluyeron ojos con DMAE exudativa previa o activa, otras enfermedades retinianas, cirugía retiniana previa, u opacidades significativas de los medios. A los 12 meses, la AVMC mejoró de 0.25 unidades logMAR (20/36) a 0.13 unidades logMAR (20/27). La sensibilidad al contraste mejoró, mientras que la estabilidad de la fijación permaneció sin cambios. TORPA 2 amplió el estudio TORPA 1 a 42 ojos. Los criterios de inclusión y exclusión fueron idénticos, con la excepción de que se incluyeron ojos con agudeza visual >20/200. A los 3 meses, se recuperaron +5.14 letras en comparación con la línea base [11,12].
5.2. Ensayos clínicos controlados
Lightwave I
Se trató de un ensayo clínico controlado de fase II, publicado en 2024, multicéntrico, con un seguimiento de 4 meses tras el uso de eye-light®. Participaron 76 pacientes (152 ojos). En cuanto a seguridad y tolerabilidad, solo el 20 % del grupo FBM reportó efectos adversos oculares leves, principalmente sensación de calor, sin comprometer la adherencia al tratamiento [8].
Respecto a la eficacia funcional, una mayor proporción del grupo FBM alcanzó una ganancia ≥5 letras (20,3 %) frente al grupo simulado (8,9 %), diferencia estadísticamente significativa (p = 0,043). En cuanto a la eficacia anatómica, no se observaron diferencias significativas en el grosor central entre los grupos a los 4 meses. Sin embargo, el volumen de drusas mostró una reducción significativa a favor del grupo FBM (p = 0,013) [8].
Lightsite I, II y III
Fueron una serie de estudios de fase I, II y III, utilizando el dispositivo Valeda®. El estudio Lightsite I, publicado en 2019, incluyó a 30 sujetos (46 ojos) con DMAE seca en categorías 2 a 4 del AREDS y AVMC basal de 20/40 a 20/200. Se incluyeron ambos ojos si cumplían los criterios de inclusión. Los participantes recibieron 3 sesiones por semana durante 3 a 4 semanas, para un total de 9 sesiones por serie, separando la segunda serie a los 6 meses [13]. Los sujetos tratados con FBM mostraron una ganancia promedio de 4 letras inmediatamente después de cada serie de tratamientos en el mes 1 y el mes 7. Aproximadamente el 50 % de los sujetos tratados con FBM mostraron una mejora de 5 letras, en comparación con el 13.6 % de los sujetos tratados con placebo en el mes 1 [13].
Lightsite II incluyó a 44 sujetos con DMAE seca (53 ojos). Los ojos tratados con FBM mostraron una mejora estadísticamente significativa en la AVMC a los 9 meses, con una ganancia de 4 letras en el grupo tratado con FBM frente a 0,5 letras en el grupo tratado con simulación para los pacientes que recibieron las 27 sesiones de FBM completas. Aproximadamente el 35,3 % de los ojos tratados con FBM mostraron una mejora ≥5 letras a los 9 meses. Aunque tanto los grupos de FBM como de simulación mostraron crecimiento de las lesiones de atrofia geográfica (AG) durante el período del ensayo, el grupo de FBM presentó un 20 % menos de crecimiento en 10 meses, lo que sugería posibles efectos modificadores de la enfermedad. Este estudio se vio afectado por la pandemia del 2020 del coronavirus, con varios sesgos metodológicos de reclutamiento de pacientes y seguimiento. Cabe mencionar que el grupo “simulado” presentó una reducción aproximada del 50 % y del 100 % en la fluencia del tratamiento, en comparación con el grupo FBM, para las longitudes de onda de 590 y 660 nm, respectivamente, además de que se omitió la longitud de onda de 850 nm. Los autores sugieren que, a pesar de esta menor intensidad, este grupo también podría haber experimentado cierta mejoría funcional [14].
Lightsite III, publicado en 2024, administró 9 sesiones de FBM durante 3 – 5 semanas, repetidas cada 4 meses. Se incluyeron a 100 sujetos (148 ojos), aleatorizados en una proporción 2:1 entre el grupo de FBM y el grupo simulado. A los 13 meses, los ojos tratados con FBM mostraron una mejora significativa en la AVMC, con una media de 5,4 letras ETDRS, en comparación con 3,0 letras en el grupo simulado, además de una reducción en la progresión hacia nueva AG con una diferencia entre grupos de 2,4 letras [6].
El estudio reportó la aparición de nueva AG en el 9,8 % de los ojos del grupo simulado y en el 1,1 % de los ojos tratados con FBM, lo que representa una reducción estadísticamente significativa en la aparición de AG en el grupo FBM. En cuanto a los efectos adversos, el 5,4 % de los ojos tratados con FBM presentó conversión a DMAE neovascular, frente al 1,8 % del grupo simulado [6].
Conclusiones
La DMAE seca sigue careciendo de tratamientos efectivos que prevengan su progresión a etapas avanzadas. La fotobiomodulación emerge como una estrategia terapéutica prometedora. sin embargo, es necesario contar con estudios adicionales, diseñados con metodologías rigurosas, que permitan validar de manera concluyente su plausibilidad biológica y su eficacia clínica, ya que, aunque la FDA reconoció una eficacia estadísticamente significativa, describió el tamaño del efecto como de relevancia clínica “marginal” y recomendó precaución debido a una posible mayor conversión a DMAE neovascular.
-
-
-
- Niels Ryberg Finsen (1860-1904) n.d. Historia de la Medicina. [Internet]. 15 octubre 2025. [Consultado 18 octubre 2025] Disponible en: https://www.historiadelamedicina.org/finsen.html
- Hamblin MR, Huang YY. Handbook of photomedicine. Handbook of Photomedicine. 2013:1–829. https://doi.org/10.1201/b15582
- Von der Burchard C, Miura Y, Stanzel B, et al. Regenerative Retinal Laser and Light Therapies (RELITE): Proposal of a New Nomenclature, Categorization, and Trial Reporting Standard. Lasers Surg Med. Wiley Online Library. [Internet]. 2024; [Consultado 21 octubre 2025] 56:693–708. Disponible en: https://doi.org/10.1002/LSM.23833
- Siqueira RC. Photobiomodulation Using Light-Emitting Diode (LED) for Treatment of Retinal Diseases. Clin Ophthalmol [Internet]. 2024; [Consultado 21 octubre 2025] 18:215–25. Disponible en: https://doi.org/10.2147/OPTH.S441962
- Valter K, Tedford SE, Eells JT, et al. Photobiomodulation use in ophthalmology – an overview of translational research from bench to bedside. Frontiers in Ophthalmology [Internet]. 2024;4. Disponible en: https://doi.org/10.3389/FOPHT.2024.1388602
- Boyer D, Hu A, Warrow D, et al. LIGHTSITE III: 13-Month Efficacy and Safety Evaluation of Multiwavelength Photobiomodulation in Nonexudative (Dry) Age-Related Macular Degeneration Using the Lumithera Valeda Light Delivery System. Retina [Internet]. 2024; [Consultado 21 octubre 2025]44:487–97. Disponible en: https://doi.org/10.1097/IAE.0000000000003980.
- Ball KA, Castello PR, Poyton RO. Low intensity light stimulates nitrite-dependent nitric oxide synthesis but not oxygen consumption by cytochrome c oxidase: Implications for phototherapy. J Photochem Photobiol B [Internet]. 2011; [Consultado 21 octubre 2025] 102:182–91. Disponible en: https://doi.org/10.1016/J.JPHOTOBIOL.2010.12.002.
- Borrelli E, Coco G, Pellegrini M, et al. Safety, Tolerability, and Short-Term Efficacy of Low-Level Light Therapy for Dry Age-Related Macular Degeneration. Ophthalmol Ther [Internet]. 2024; [Consultado 21 octubre 2025]13:2855–68. Disponible en: https://doi.org/10.1007/S40123-024-01030-W
- Lu YZ, Natoli R, Madigan M, et al. Photobiomodulation with 670 nm light ameliorates Müller cell-mediated activation of microglia and macrophages in retinal degeneration. Exp Eye Res [Internet]. 2017; [Consultado 21 octubre 2025]165:78–89. Disponible en: https://doi.org/10.1016/j.exer.2017.09.002.
- Begum R, Powner MB, Hudson N, et al. Treatment with 670 nm light up regulates cytochrome C oxidase expression and reduces inflammation in an age-related macular degeneration model. PLoS One [Internet]. 2013;8. Disponible en: https://doi.org/10.1371/JOURNAL.PONE.0057828.
- Merry G, Dotson R, Devenyi R, et al. Photobiomodulation as a New Treatment for Dry Age Related Macular Degeneration. Results from the Toronto and Oak Ridge Photobimodulation Study in AMD (TORPA). Invest Ophthalmol Vis Sci 2012; 53:2049–2049.
- Merry GF, Munk MR, Dotson RS, et al. Photobiomodulation reduces drusen volume and improves visual acuity and contrast sensitivity in dry age-related macular degeneration. Acta Ophthalmol [Internet]. 2017; [Consultado 21 octubre 2025] 95:e270–7. Disponible en: https://doi.org/10.1111/AOS.13354.
- Markowitz SN, Devenyi RG, Munk MR, et al. A DOUBLE-MASKED, RANDOMIZED, SHAM-CONTROLLED, SINGLE-CENTER STUDY WITH PHOTOBIOMODULATION FOR THE TREATMENT OF DRY AGE-RELATED MACULAR DEGENERATION. Retina [Internet]. 2020; [Consultado 21 octubre 2025] 40:1471–82. Disponible en: https://doi.org/10.1097/IAE.0000000000002632.
- Burton B, Parodi MB, Jürgens I, et al. LIGHTSITE II Randomized Multicenter Trial: Evaluation of Multiwavelength Photobiomodulation in Non-exudative Age-Related Macular Degeneration. Ophthalmol Ther [Internet]. 2023; [Consultado 21 octubre 2025] 12:953–68. Disponible en: https://doi.org/10.1007/S40123-022-00640-6.
-
-